一起吃饭、游泳会感染艾滋病、乙肝、丙肝病毒吗?科学研究带你破除认知误区!|健康素养66条
来源:CHTV百姓健康2025-11-29 19:27:06
他/她查出乙肝了,以后还能一起吃饭吗?与人类免疫缺陷病毒(HIV)携带者牵手拥抱会被传染吗?在公共泳池游泳会感染艾滋病、乙肝、丙肝病毒吗?这些充满焦虑的提问,在世界艾滋病日来临之际,依然频繁出现在基层诊室的咨询台、社交媒体和健康热线的另一端。

截至2025年,全国现存HIV感染者及AIDS患者已达1,387,471例,累计死亡超50万例。作为乙类传染病发病数的榜首,病毒性肝炎在2025年10月的发病数高达116,746例,占所有乙类传染病的44.2%[1]。其中丙肝虽然发病数低于乙肝,但致死率却更高。
12月1日是世界艾滋病日,我们有必要重温《中国公民健康素养——基本知识与技能(2024年版)》第11条:艾滋病、乙肝和丙肝仅通过血液、性接触和母婴三种途径传播,日常生活和工作接触不会感染。然而,纸面上的科学共识与人们内心深处的担忧之间,依然横亘着一条需要被跨越的信任鸿沟。为何在信息如此发达的今天,关于传播途径的基础认知仍存在如此大的鸿沟?
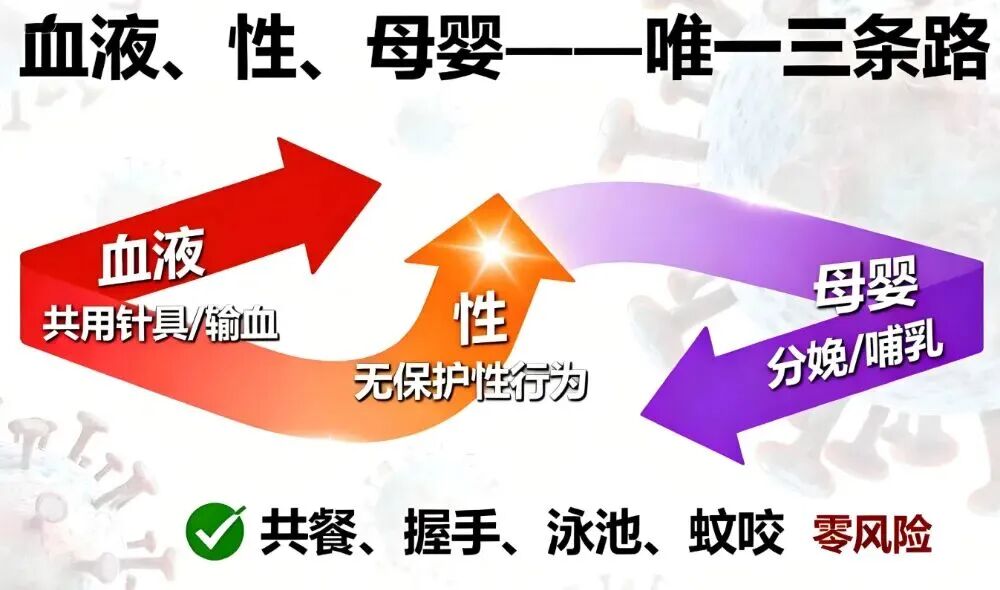
消除不必要的恐惧:
三类途径明确,日常接触无风险
被误解的日常
艾滋病、乙肝和丙肝的传播途径高度特定,病毒传播必须同时满足三个条件:足量活病毒、有效排出途径、直接进入易感者血液循环。研究显示,乙肝病毒在体外干燥环境中可存活7天,丙肝病毒存活时间约1-4天,HIV在干燥血液中1-2小时即失去感染性[2]。在口腔中黏膜完整,无破损和溃疡的情况下,唾液中病毒含量较低,远未达到感染所需阈值;而HIV无法在消化道存活,乙肝和丙肝病毒也无法在胃酸环境中保持活性,且口腔黏膜和消化酶会进一步降解病毒,形成双重防护[3]。
一项回顾性定群研究同样印证了这一点,研究分析了117例因输血引入HIV的家庭、487名成员,平均共同生活8.1年。146名无夫妻/母婴传播危险因素的家庭成员中,HIV抗体检测全部阴性,提示日常接触未发生感染[4]。
U=U(Undetectable = Untransmittable):治疗即预防的革命
检测不到=不传染(U=U)这一概念,已成为艾滋病防治领域近年来十分具革命性的突破。2019年完成的PARTNER2研究发表于The Lancet,追踪了972对男男性行为伴侣(其中一方为HIV阳性且接受抗病毒治疗),在累计超过7.6万次无保护性行为后,未发生一例HIV传播,前提是阳性方病毒载量持续低于200 copies/mL[5]。也就是当HIV感染者接受有效的抗病毒治疗并维持病毒载量检测不到时,通过性接触传播HIV的风险极低。

这一结果奠定了“U=U”的科学共识,并被WHO及我国《艾滋病诊疗指南(2024版)》正式采纳。这意味着,规范治疗的HIV感染者,其性传播风险接近为零。这对消除歧视、促进治疗依从性具有革命性意义。
乙肝方面,虽然尚无“U=U”概念,但高敏HBV DNA检测显示,当病毒载量低于2000 IU/mL时,性传播风险极低;而经母婴阻断(孕期抗病毒+新生儿免疫球蛋白+疫苗),传播率已从20%降至1%以下[6]。丙肝则更为乐观——由于HCV主要通过血液传播,且无慢性携带状态(治愈即清除),只要避免共用针具、确保医疗器械消毒,社区传播几乎可防可控。最有力的是,我们拥有高效的乙肝疫苗,成功接种后可提供至少二十年的保护,是预防乙肝最可靠的盾牌。
重新认识真正的风险
相比之下,乙肝病毒在环境中的存活能力更强,在干燥环境下可存活长达7天。这解释了为什么共用可能接触血液的个人物品(如剃须刀、牙刷)具有潜在风险。而丙肝的传播则主要与直接血液接触相关,如未经严格消毒的文身、穿刺器械或注射吸毒。
值得注意的是,2024年发表于PLoS Pathog一项的猕猴实验(PMC11623940),研究人员经直肠(IR)给非洲绿猴(AGM)接种 SIVsab,观察接种后2–3天血浆病毒RNA阳性,发现病毒在接种后24–48h即可通过淋巴途径进入血流,局部复制与系统播散几乎同时发生,提示病毒几乎同步完成肠道-血液-全身播散,干预窗口极短甚至不存在[7]。

治疗前沿:
根治仍是梦想,但功能性治愈已触手可及
回到最初的那些问题,人们真正担忧的或许不是会不会传染,而是“得了是不是就没救了”。这也是本文需要传递的关键信息:HIV、HBV、HCV虽机制不同,但治疗前景远比公众想象的光明。

而乙肝的治疗目标也已从病毒抑制升级为功能性治愈,欧洲肝脏研究学会(EASL)指南把“功能性治愈(HBsAg持续阴转伴或不伴抗-HBs阳转)”列为部分患者可实现的终点,推荐优先用于“HBsAg<1500 IU/mL、HBeAg阴性、年轻、无肝硬化”人群。此外,2025年发表于Frontiers in Medicine的多中心回顾性研究(n=122)发现,Peg-IFNα联合核苷类似物治疗48周,基线HBsAg<1500 IU/L患者的HBsAg清除率为40.98%,单用核苷组为0%(P<0.001),为功能性治愈提供了新路径,临床医生可以定期为患者监测HBsAg定量,及时调整治疗方案[9,10]。
最后说到最难破解的难题——HIV根治仍面临潜伏库的挑战,但功能性治愈探索已取得重要进展,长效疗法更改写了治疗模式。2025年CROI会议公布的Ⅱ期研究显示,由来那卡韦(Lenacapavir)和广谱中和抗体组成的长效方案,每6个月给药一次,即可使90%以上患者HIV RNA持续低于检测下限。在治愈方面,南非2025年公布的临床试验初步结果显示,12例接受造血干细胞移植联合免疫调节的患者中,3例停药24周后未出现病毒反弹,这为治愈艾滋病带来了新曙光[11-13]。
远离可怕的病毒:如何科学防护?
1、普通人群:厘清风险边界,消除认知误区
无需恐慌日常接触:共餐、握手、拥抱、共用办公用品等行为一般不会传播艾滋病、乙肝或丙肝。
关键防护措施:避免共用剃须刀、牙刷等可能接触血液的个人物品。文身、穿刺等选择正规机构,确保器械严格消毒。接种乙肝疫苗是预防乙肝最有效的手段。
2、高风险人群:强化药物预防+定期筛查
艾滋病暴露前预防(PrEP):存在艾滋病暴露风险的人员(如高风险行为者),应主动寻求专业评估。在医生指导下规范使用暴露前预防药物,并坚持使用安全套,可建立双重保障,显著降低感染风险。
定期筛查:建议高风险人群每3-6个月进行HIV、丙肝抗体和乙肝标志物检测。
3、感染者与患者:积极治疗,阻断传播
艾滋病“U=U”共识:当HIV感染者接受有效抗病毒治疗且病毒载量持续检测不到时,通过性接触传播HIV的风险下降几乎为零。这是赋予感染者尊严、消除社会歧视的强大科学武器。但是与此同时,从公共卫生和个人全面防护的角度出发,仍建议使用安全套,这能作为一道额外屏障,确保在病毒载量可能发生未知波动(如因断药、耐药)时,依然可以起到保护作用。
乙肝病毒抑制:有效的抗病毒治疗可以显著降低乙肝病毒感染者的病毒水平,从而大幅降低传播风险。
丙肝治愈终结传播:丙肝患者治愈后,其传播风险也随之归零。

4、母婴阻断:成功率可达99%
艾滋病:通过抗病毒治疗+安全分娩+人工喂养全程规范干预综合策略,母婴传播率可降至1%以下。
乙肝:新生儿在出生后24小时内接种乙肝疫苗和乙肝免疫球蛋白,阻断成功率高达99.3%。对于高病毒载量的孕妇,妊娠晚期可进行抗病毒药物干预,进一步降低宫内感染风险。
结语:
用科学证据驱散恐惧
以医学进步传递希望
参考文献:
[1] 国家疾病预防控制局. 2025年10月全国法定传染病疫情概况[A/OL]. 北京: 国家疾病预防控制局, 2025[2025-11-30]. http://www.ndcpa.gov.cn/jbkzzxs/tjxx/202511/t20251128_000001.html.
[2] Centers for Disease Control and Prevention. Survival of HIV, HBV and HCV in the environment and risk of environmental transmission[A/OL]. Atlanta: CDC, 2024[2025-11-30].
[3] 卫生部办公厅 教育部办公厅关于印发《青少年预防艾滋病基本知识》的通知 - 中华人民共和国教育部政府门户网站
[4] 陈素良, 赵宏儒, 张玉琪,等. 未知情家庭艾滋病传播回顾性定群研究. 中国公共卫生, 2009, 25(7): 790-791.
[5] Rodger AJ, Cambiano V, Bruun T,et al. Risk of HIV transmission through condomless sex in serodifferent gay couples with the HIV-positive partner taking suppressive antiretroviral therapy (PARTNER): final results of a multicentre, prospective, observational study[J]. Lancet. 2019 Jun 15;393(10189):2428-2438. Doi: 10.1016/S0140-6736(19)30418-0.
[6] Funk AL, Lu Y, Yoshida K,et al. Efficacy and safety of antiviral prophylaxis during pregnancy to prevent mother-to-child transmission of hepatitis B virus: a systematic review and meta-analysis[J]. Lancet Infect Dis. 2021 Jan;21(1):70-84. Doi: 10.1016/S1473-3099(20)30586-7.
[7] Raehtz KD, Xu C, Deleage C,et al. Rapid systemic spread and minimal immune responses following SIVsab intrarectal transmission in African green monkeys[J]. JCI Insight. 2024 Dec 6;9(23):e183751. Doi: 10.1172/jci.insight.183751.
[8] Cooke GS, Hung LM, Flower B,et al. Treatment options to support the elimination of hepatitis C: an open-label, factorial, randomised controlled non-inferiority trial[J]. Lancet. 2025 May 17;405(10491):1769-1780. Doi: 10.1016/S0140-6736(25)00097-2.
[9] Peng Y, Ma MZ, Liu T, et al. Predictors of HBsAg seroclearance in HBeAg-negative chronic hepatitis B patients treated with nucleotide analogs plus polyethylene glycol interferon[J]. Frontiers in Medicine (Lausanne). 2025 Jan 8;11:1510230.
[10]Zhang S, Wang J, Jiang C, et al. Treatment coverage of the WHO 2024 hepatitis B guidelines in patients with chronic hepatitis B. EASL2025, Abstract (SAT-318-YI).
[11]Kwadwo Mponponsuo, James H. McMahon, Linda Gorgos, et al. Efficacy and Safety of Lenacapavir, Teropavimab, and Zinlirvimab: Phase II Week 26 Primary Outcome. CROI 2025; Abstract 151.
[12]Luise Rogg, Sebastián A. Núñez, Maria Verónica Mingrone, et al. Proof-of-Concept Trial of VH4524184 (VH-184), a Third-Generation Integrase Strand Transfer Inhibitor. CROI 2025; Abstract 152.
[13]Rulan Griesel, Sebastián A. Núñez, Alma Minerva Pérez Rios, et al. Proof-of-Concept Trial of Oral VH4011499 (VH-499), a New HIV-1 Capsid Inhibitor. CROI 2025; Abstract 153.

 CHTV 百姓健康微信
CHTV 百姓健康微信